摘要 / TL;DR
性激素(如睾酮,雌二醇)与血蛋白(如白蛋白, SHBG)结合。 这减少了其游离部分,从而限制了其生物活性。 雄激素减少 SHBG 的产生,而雌二醇增加 SHBG 的产生,因此睾酮和雌二醇可以影响到各自的游离部分。 由于肝脏的强烈灭活作用,正常情况下,睾酮和雌二醇对 SHBG 的影响相当小。 但在很高水平时,它们能显著地影响 SHBG 的水平。 怀孕时雌二醇的水平极大地增加(例如,100 倍),SHBG 水平最高可提高 5 ~ 10 倍。 尽管大量增加的 SHBG 水平能强烈地抑制睾酮的生物活性,但对雌二醇却有所不同。 在怀孕后期,游离雌二醇的百分比似乎只降到非妊娠时的一半左右。 怀孕初期—雌二醇水平低一些—游离雌二醇却减少到更少的程度。 在女性化激素治疗的典型雌二醇水平下,SHBG 对游离雌二醇的限制作用很小。 口服雌二醇对 SHBG 产生的影响大于非口服雌二醇,这或许会使口服与非口服雌二醇出现不同的效果,但口服雌二醇最终的活性较低只是理论上的,现有的临床研究未曾报道与非口服雌二醇有关的重要治疗差异。 总而言之,尽管 SHBG 的增加会减少游离雌二醇的百分比,女性倾向跨性别者不必太担心 SHBG 对雌二醇的有效性的影响。
性激素对血蛋白的结合
性激素与血液中名为血浆蛋白的蛋白结合。这一现象被称为血浆蛋白结合。至于雄激素和雌激素,它们主要与白蛋白和性激素结合球蛋白( SHBG )。血浆蛋白结合起到防止性激素与其靶细胞相互作用,从而防止结合和激活其受体结( Hammond, 2016 )。这是因为血浆蛋白太大又不溶于脂而不能穿过富脂的细胞膜。结果,它们不能穿透毛细血管退出血液循环或进入组织或被细胞吸收。当性激素与血浆蛋白结合,它也不能进入靶细胞。因此,血浆蛋白结合限制了性激素的生物活性( Hammond, 2016 )。与血浆蛋白结合也起到延长性激素的生物半衰期,因为与蛋白质结合的性激素同样地不能被代谢,也无法进行依赖于细胞吸收的清除。
每个 SHBG 分子仅有一个性激素结合位点( Moore & Bulbrook, 1988 ),而白蛋白有六个针对不同底物的结合位点( Pardridge, 1988 )。雄激素和雌二醇对 SHBG 有高亲和力( nM ),而对白蛋白有低亲和力( μM ) ( Moore & Bulbrook, 1988; Hammond, 2016 )。但是,白蛋白水平比 SHBG 水平高上几个数量级( μM vs. nM ),这起到平衡各蛋白与性激素结合的部分( Hammond, 2016 )。雄激素对 SHBG 的亲和力高于雌二醇或其他的雌激素。雌二醇对 SHBG 的亲和力仅有双氢睾酮( DHT )的 10%~ 20% ,或睾酮的 33%~ 50%( Anderson, 1974; Ojasoo & Raynaud, 1978; Pugeat, Dunn, Nisula, 1981 )。因此,睾酮和 DHT 与 SHBG 结合得比雌二醇更牢。
血液中的绝大多数性激素与血浆蛋白结合;在任何时刻,血液中 97% 以上的睾酮,雌二醇和孕酮与血浆蛋白结合( Strauss & FitzGerald, 2019 )。未与血浆蛋白结合的那部分性激素称为游离部分或未结合部分。这部分能透入细胞,因此被认为具有生物活性( Hammond, 2016 )。总水平指游离/未结合和结合的激素两者之和。生物可用水平包含白蛋白结合的激素和游离激素水平。由于它们对白蛋白的亲和力相当的弱,与白蛋白结合的性激素可能具有一定程度的生物活性—因此,所以用「生物可用」修饰( Nguyen et al., 2008 )。不过,需要更多的研究来全面地阐明与血蛋白结合的部分性激素的生物活性。
雌二醇,睾酮和 DHT 与白蛋白,SHBG 和另一种血浆蛋白皮质类固醇结合球蛋白( CGB )(只与少量睾酮结合,不与雌二醇结合)结合的百分比和游离的百分比已大致算出。见下表。
表 1:计算出的性激素与血浆蛋白结合( Dunn, Nisula, & Rodbard, 1981 ):
| 激素 | 组 | 白蛋白 (%) | SHBG (%) | CBG (%) | 游离 (%) |
|---|---|---|---|---|---|
| 雌二醇 | 女性 (卵泡期) | 60.8 | 37.3 | <0.1 | 1.81 |
| 女性 (黄体期) | 61.1 | 37.0 | <0.1 | 1.82 | |
| 女性 (妊娠) | 11.7 | 87.8 | <0.1 | 0.49 | |
| 男性 | 78.0 | 19.6 | <0.1 | 2.32 | |
| 睾酮 | 女性 (卵泡期) | 30.4 | 66.0 | 2.26 | 1.36 |
| 女性 (黄体期) | 30.7 | 65.7 | 2.20 | 1.37 | |
| 女性 (妊娠) | 3.60 | 95.4 | 0.82 | 0.23 | |
| 男性 | 49.9 | 44.3 | 3.56 | 2.23 | |
| DHT | 女性 (卵泡期) | 21.0 | 78.4 | 0.12 | 0.47 |
| 女性 (黄体期) | 21.3 | 78.1 | 0.12 | 0.48 | |
| 女性 (妊娠)) | 2.15 | 97.8 | 0.04 | 0.07 | |
| 男性 | 39.2 | 59.7 | 0.22 | 0.88 |
游离性激素水平和百分比常常是用总性激素水平,白蛋白水平,SHBG 水平,和 CGB 水平按一确证的数学模型(从已发行的研究的数据构建)计算得来。这因为游离激素水平通常很低( pM 范围),很难用常规的血检方式测量。尽管总体上在真实值附近,算出的结果不总是完全准确( Rosner, 2015; Goldman et al., 2017; Handelsman, 2017; Keevil & Adaway, 2019 )。因此,行得通时,尽可能使用测量水平。
性激素对 SHBG 产生的影响
血浆蛋白(如白蛋白,SHBG )在肝脏中合成并分泌到血液中。除了与 SHBG 结合,性激素还调节肝脏产生 SHBG ,从而影响到它们各自的血浆蛋白结合。雄激素减少 SHBG 的产生,而雌激素增加 SHBG 的产生( Anderson, 1974; Moore & Bulbrook, 1988 )。服用合成代谢类固醇 stanozolol (一种合成 DHT 衍生物)几天就可抑制达 63% 的 SHBG 水平( Krause et al., 2004 )。持续使用极大剂量的睾酮和其他合成代谢类固醇能降低 90% 的 SHBG 水平( Ruokonen et al., 1985; Moore & Bulbrook, 1988 )。类似地,弱雄激素性孕激素,如醋酸甲羟孕酮( MPA ),炔诺酮( NET )和左炔诺孕酮( LNG ),会降低 SHBG 产生( Kuhl, 2005 ),非常高剂量的醋酸甲羟孕酮和 醋酸甲地孕酮( MGA )被报道会降低高达约 50 ~ 90% 的 SHBG 水平( Heubner et al., 1987; Lundgren et al., 1990; Lundgren & Lønning, 1990 )。与此相反,含有合成雌激素炔雌醇(及少许雄激素性或抗雄激素性孕激素)的避孕药增加约 4 倍的 SHBG 水平( Odlind et al., 2002 )。高剂量的口服合成雌激素曾加 SHBG 水平高达 5 ~ 10 倍( von Schoultz et al., 1989 )。
睾酮,DHT 和雌二醇被肝脏强烈地灭活,在正常情况下,对身体这部分的影响相当的弱。因此,它们对 SHBG 生产的影响相对于合成激素类药物来讲较小。 因此,尽管在整个月经周期中雌二醇水平的波动很大,SHBG 的水平仅稍微变化了一点点( Freymann et al., 1977b; Plymate et al., 1985; Schijf et al., 1993; Braunstein et al., 2011; Rothman et al., 2011; Fanelli et al., 2013; Rezaii et al., 2017 )。在一项研究中,从卵泡期过渡到黄体期时,SHBG 水平增加了约 6 ~ 13% (+2.9–5.3 nmol/L)( Braunstein et al., 2011 )。此外,更年期时雌二醇急剧减少,SHBG 水平仅降低少许( Burger et al., 2000; Guthrie et al., 2004 )。尽管如此,在特定的条件下,雌二醇疗法还是能明显地影响 SHBG 的生产及其他肝蛋白( Kuhl, 1998 )。 这是由于 1)使用口服雌二醇,这是因为肝的首过对雌激素敏感的肝脏分泌的影响比非口服途径大( Kuhl, 2005 );2)使用高剂量雌二醇,例如典型的注射剂量。下表展示了从许多不同的研究不同雌激素途径,剂量和种类中得出的 SHBG 增加。
表 2:在不同的雌二醇暴露下 SHBG 水平的相对增加
| 雌激素 | 典型 E2 水平 a | SHBG 增加 | 来源 |
|---|---|---|---|
| Oral E2 1 mg/day | ~25 pg/mL | 1.6× | Kuhl (1998) |
| Oral E2 2 mg/day | ~50 pg/mL | 2.2× | Kuhl (1998) |
| Oral E2 4 mg/day | ~100 pg/mL | 1.9–3.2× | Fåhraeus & Larsson-Cohn (1982); Gibneyet al. (2005); Ropponen et al. (2005) |
| Oral EV 6 mg/dayb | ~112.5 pg/mL | 3.0× | Dittrich et al. (2005) |
| E2 patch 50 μg/day | ~50 pg/mL | 1.1× | Kuhl (2005) |
| E2 patch 100 μg/day | ~100 pg/mL | 1.2× | Shifren et al. (2008) |
| E2 patches 200 μg/day | ~200 pg/mL | ~1.5× | Smith et al. (2019) |
| E2 patches 300 μg/day | ~300 pg/mL | ~1.7× | Smith et al. (2019) |
| E2 patches 600 μg/day | ~600 pg/mL | 2.3× | Bland et al. (2005) |
| EU 100 mg/month | ~550 pg/mL | 2.0× | Derra (1981) |
| PEP 320 mg/month | ~700 pg/mL | 1.7× | Stege et al. (1988) |
| EV 10 mg/10 days | Variable (high) | 3.2× | Mueller et al. (2011) |
| Oral EE 10 μg/day | – | 3.0× | Kuhl (1998) |
| Oral EE 50 μg/day | – | 4.0× | Kuhl (1997) |
| 高剂量合成雌激素 | – | 5–10× | von Schoultz et al. (1989) |
a 从多种来源估计的典型雌二醇水平( e.g., Wiki; Aly, 2020 )。 b由于分子质量不同,EV 只有平常雌二醇约 75% 的雌二醇的量。因此,6 mg/day EV 约等于 4.5 mg/day E2 。
雌二醇对 SHBG 水平的影响与妊娠联系最密切,此时雌二醇水平升至远高与平常水平。在妊娠后期,雌二醇水平通常平均在约 15,000 至 25,000 pg/mL 之间( Graphs; Troisi et al., 2003; Adamcová et al., 2018 )。这些雌二醇水平是正常月经周期雌二醇水平的 100 倍。到妊娠后期,雌二醇水平大量增加的同时,SHBG 水平增加约 5 ~ 10 倍( Anderson, 1974; Hammond, 2017 )。雌激素和 SHBG 生产的剂量-反应曲线显示了其饱和度,大部分的 SHBG 水平增长发生在较低的雌二醇水平及 SHBG 水平能升至多高的限制( Mean, Pellaton, & Magrini, 1977; O’Leary et al., 1991; Kerlan et al., 1994; Kuhl, 1999 )。下图展示了整个妊娠时 SHBG 水平。
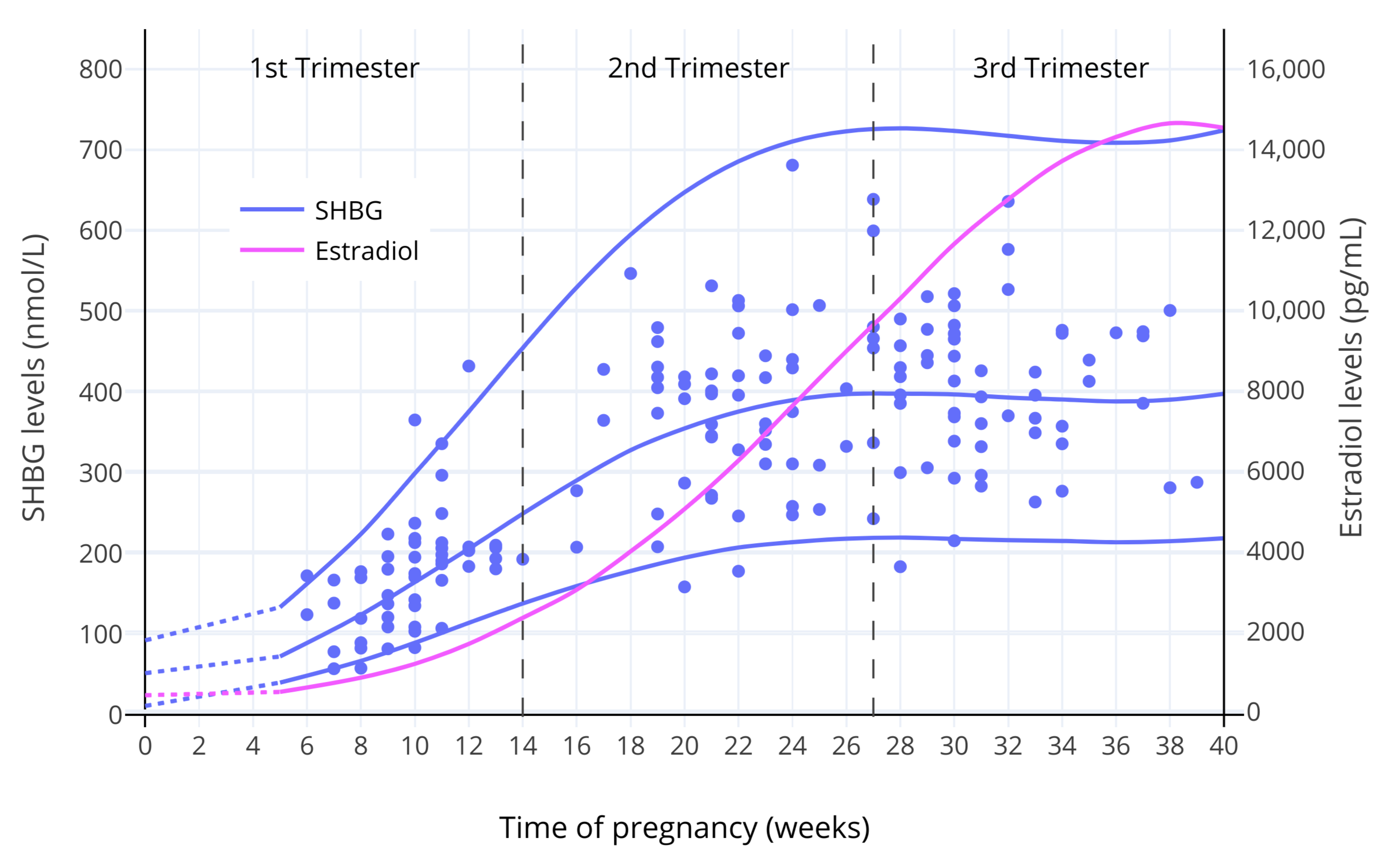
图 1:妊娠期间,SHBG 和总雌二醇的水平(O’Leary et al., 1991)。线代表平均值和/或第 95 百分位数,而点表示单独的测量值。
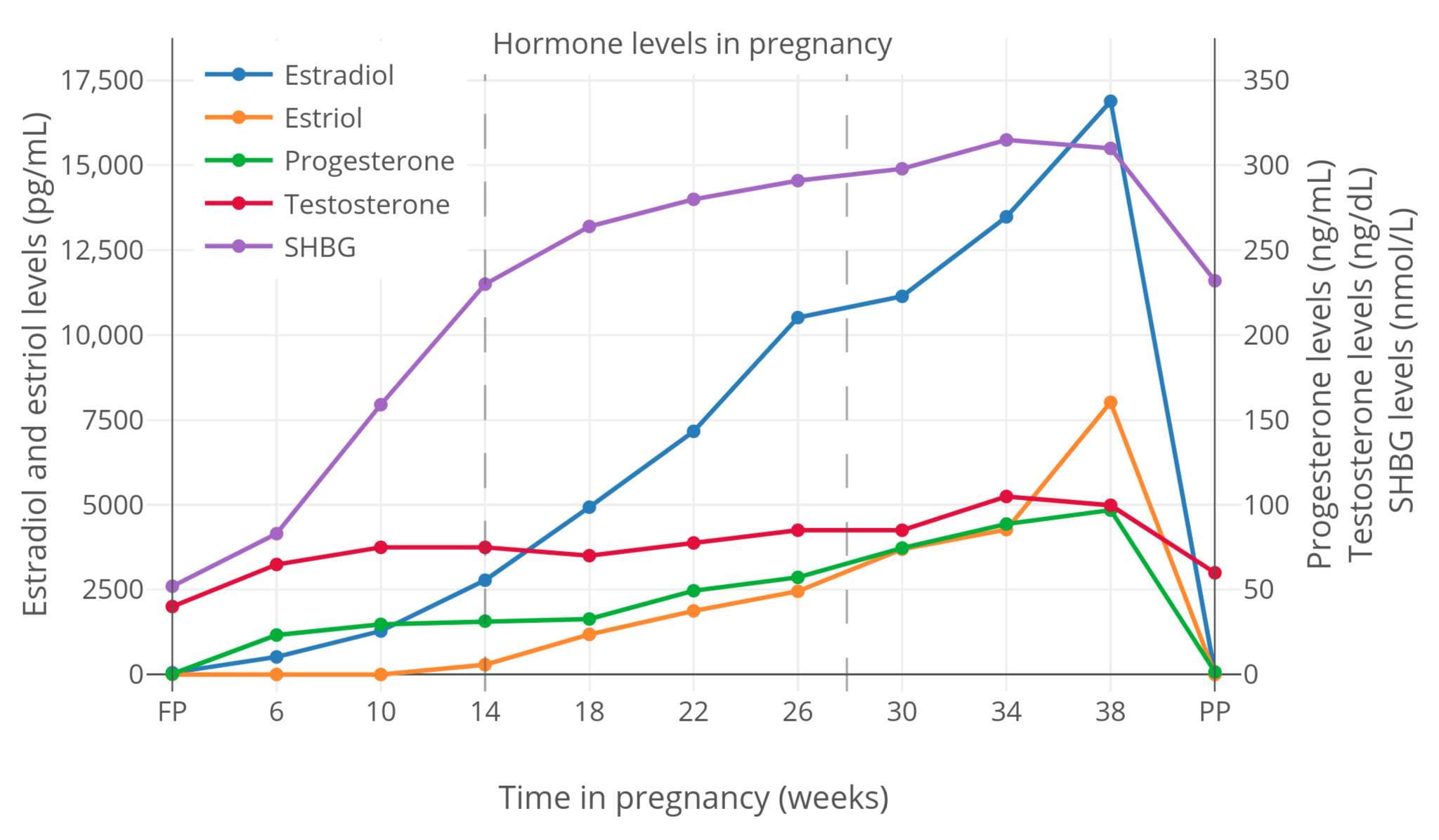
图 2:女性妊娠期间,总性激素和 SHBG 水平(Kerlan et al., 1994)。
SHBG 增加对游离性激素水平的影响
SHBG 水平的变化导致了与 SHBG 结合的性激素水平和游离性激素的改变。除了 DHT 外,雌二醇和睾酮是在这一方面有最大关系的性激素。
SHBG 增加与游离睾酮
含有 EE 的避孕药,会使 SHBG 水平增长 4 倍,能显著地降低游离睾酮的百分比(Graham et al., 2007; Zimmerman et al., 2014)。在一项研究中,一片含有 EE 的避孕药使游离睾酮的百分比从 2.45% 降至 0.78% (降低 3.2 倍或降至基线的 32%)(Graham et al., 2007)。由于同时抑制了睾酮的产生,从而降低了总睾酮水平,游离睾酮水平从 0.89 pg/mL 降至 0.18 pg/mL (降低 5 倍,至基线的 20%)(Graham et al., 2007)。含有 EE 的避孕药对 SHBG 水平的影响显著地增强了其抗雄作用,这被用来治疗女性痤疮和多毛症。
怀孕时,睾酮水平可升至高达 150 ng/dL (约 5 倍于非孕期水平)( McClamrock, 2007 )。妊娠时增加的 SHBG 生产起到了降低升高的睾酮水平的生物活性这一重要作用( Hammond, 2017 )。在一项研究中,游离睾酮的百分比在妊娠后期时比非孕期时低六倍( 0.23% vs. 1.36%—或低至非孕期时的 17% )( Dunn, Nisula, & Rodbard, 1981 )。由此,尽管怀孕时总睾酮水平大量增加,游离睾酮水平,或近一步讲,身体里的雄激素作用几乎不变( Barini, Liberale, & Menini, 1993; Schuijt et al., 2019 )。一例因 SHBG 严重不足而出现严重的雄激素增多症的孕妇证实了 SHBG 在这段时间里限制睾酮发挥雄激素作用的作用( Hogeveen et al., 2002; Hammond, 2017 )。
SHBG 增加和游离雌二醇
内源和非口服雌二醇
研究表明,生理水平下的雌二醇(如 <200 pg/mL )受 SHBG 水平增加而降低游离雌二醇的影响甚微。只要是非口服途径,无论内源的还是外源的雌二醇都是这样。这样的结论是由计算出的和测量出的游离雌二醇的研究两者得出的。( e.g., Freymann et al., 1977b )。
不过,受 SHBG 水平增加而降低游离雌二醇这一表现在超生理水平的雌二醇下(如孕期或使用超高剂量的雌二醇疗法)变得更明显。很少有人研究高剂量的雌二醇下游离雌二醇的变化,与计算出的游离雌二醇研究相比,测量出的游离雌二醇研究更是如此。不管怎样,我们可以从孕妇身上了解游离雌二醇与高雌二醇水平间的关系。此外,由于怀孕时雌二醇水平非常高,游离雌二醇在这期间更容易检测,因此,有许多妊娠时测量出游离雌二醇的研究。
虽然游离雌二醇百分比在怀孕期间降低了,增加的雌二醇远比被 SHBG 中和的多。因此,妊娠时,游离雌二醇的变化与游离睾酮的变化并不相同。下面一摘录是对此的描述( Rubinow et al., 2002 ):
妊娠伴随着血浆中许多类固醇和肽类激素水平缓慢但持续的增长,并在分娩后的几天里急剧下降。到第三孕期时,血浆中孕酮水平平均约为 150 ng/ml ,雌二醇水平在 10 到 15 ng/ml 之间。这些量分别相当于月经周期最大值的 10 倍和 50 倍( Tulchinsky et al., 1972 )。尽管这些类固醇只有一小部分未结合,「游离」(具有生物活性)的孕酮和雌激素在妊娠期间也同样地大量增加了( Heidrich et al., 1994 )。
在这一摘录中引用的 Heidrich 及其同事的研究中,分娩时的总雌二醇水平是 21,500 pg/mL 测出的游离雌二醇水平是 232 pg/mL ,游离雌二醇为 1.08% ( Heidrich et al., 1994 )。作为对比,非孕期女性的游离雌二醇的百分比在 1.5 到 2.1% 之间(使用 RIA 测量),而游离雌二醇水平为 0.30 至 4.1 pg/mL (使用 RIA 测量)或 0.40 至 5.9 pg/mL (使用 LC–MS/MS 测量)( Jameson & De Groot, 2015 )。 因此,在这项研究中,妊娠后期的游离雌二醇水平比非孕期时最高水平高约 50 倍。
由于检测方法的不同,单一研究的发现可能不具代表性,因此,下表提供了几项不同的研究中测出的妊娠后期游离雌二醇的百分比。
表 3:测出的妊娠后期游离雌二醇百分比(平均值 ± 标准差)( Perry et al., 1987 ):
| 研究 | 方式 | n | 游离 E2 (%) |
|---|---|---|---|
| Perry et al. (1987) | 离心超滤 | 25 | 1.27 ± 0.23 |
| Hammond et al. (1980) | 离心超滤 | 5 | 0.96 ± 0.12 |
| Heidrich et al. (1994) | 离心超滤 | 26 | 1.08 |
| Tulchinsky et al. (1973) | 平衡透析 | 5 | 0.67 ± 0.18 |
| Freymann et al. (1977a) | 平衡透析 | 17 | 1.15 |
| Anderson et al. (1986) | 稳态凝胶过滤 | 12 | 1.48 ± 0.55 |
从表中可知,妊娠后期的游离雌二醇百分比大约在 0.7 到 1.5% 之间。使用计算出的妊娠后期游离雌二醇水平的研究得出的结果和测量出的相近,虽然相较而言,有时要低一点点(如 0.5% )( Dunn, Nisula, & Rodbard, 1981; Campino et al., 2001 )。这些妊娠后期测出的游离雌二醇百分比可以慎重地与百分比为 1.5 到 2.1% 的非孕期妇女进行比较。使用这些范围的中间值,妊娠后期的游离雌二醇百分比大致为非孕期的 60% 。这一估计值与一项研究的发现(游离雌二醇的百分比降至非孕期的 55% )相当接近( Freymann et al., 1977a; Freymann et al., 1977b )。
与雌二醇相反,雌酮和雌三醇的游离百分比在妊娠后期和非孕期并无区别( Tulchinsky & Chopra, 1973; Steingold et al., 1987 )。这是由于雌酮和雌三醇对 SHBG 的亲和力远低于雌二醇的( Kuhl, 2005 )。
研究也评定了妊娠早期的游离雌二醇百分比—理论上与妊娠后期不同。一项测定了整个孕期的游离雌二醇的研究的结果已在下表中( Freymann et al., 1977a; Freymann et al., 1977b )。
表 4:妊娠时,总雌二醇和游离雌二醇(平均值 ± 标准差)( Freymann et al., 1977a/b ):
| Context | n | E2 (ng/mL) | Change | Free E2 (%) | Change | Free E2 (pg/mL) | Change |
|---|---|---|---|---|---|---|---|
| Non-pregnant | 35 | 0.16 ± 0.10 | 1.0× | 2.2 ± 0.4 | –0% | 3.5 ± 2.0 | 1.0× |
| Pregnancy | |||||||
| 6–20 weeks | 9 | 2.0 ± 1.1 | 13× | 1.6 ± 0.4 | –27% | 32 ± 21 | 9.1× |
| 12–20 weeks | 10 | 5.5 ± 2.2 | 34× | 1.3 ± 0.3 | –41% | 72 ± 39 | 21× |
| 20–30 weeks | 12 | 10.8 ± 4.6 | 68× | 1.2 ± 0.3 | –45% | 130 ± 74 | 37× |
| 30–38 weeks | 17 | 16.0 ± 7.0 | 100× | 1.2 ± 0.2 | –45% | 184 ± 103 | 53× |
在一项由另一群研究者开展的相似的研究中,游离雌二醇在妊娠早期测量( 7–16 周),得出的数据比 Freymann 及其同事得出的低( Bernstein et al., 1986; Depue et al., 1987; Bernstein et al., 1988 )。游离雌二醇百分比在 10 周时约为 0.9 或 1.0% ,在 12 周时约为 0.7% ( Bernstein et al., 1986; Depue et al., 1987; Bernstein et al., 1988 )。由此,与 Freymann 及其同事的结果一样,游离雌二醇百分比随着妊娠的进展而降低。下图以可视化的形式展示了这一发现。
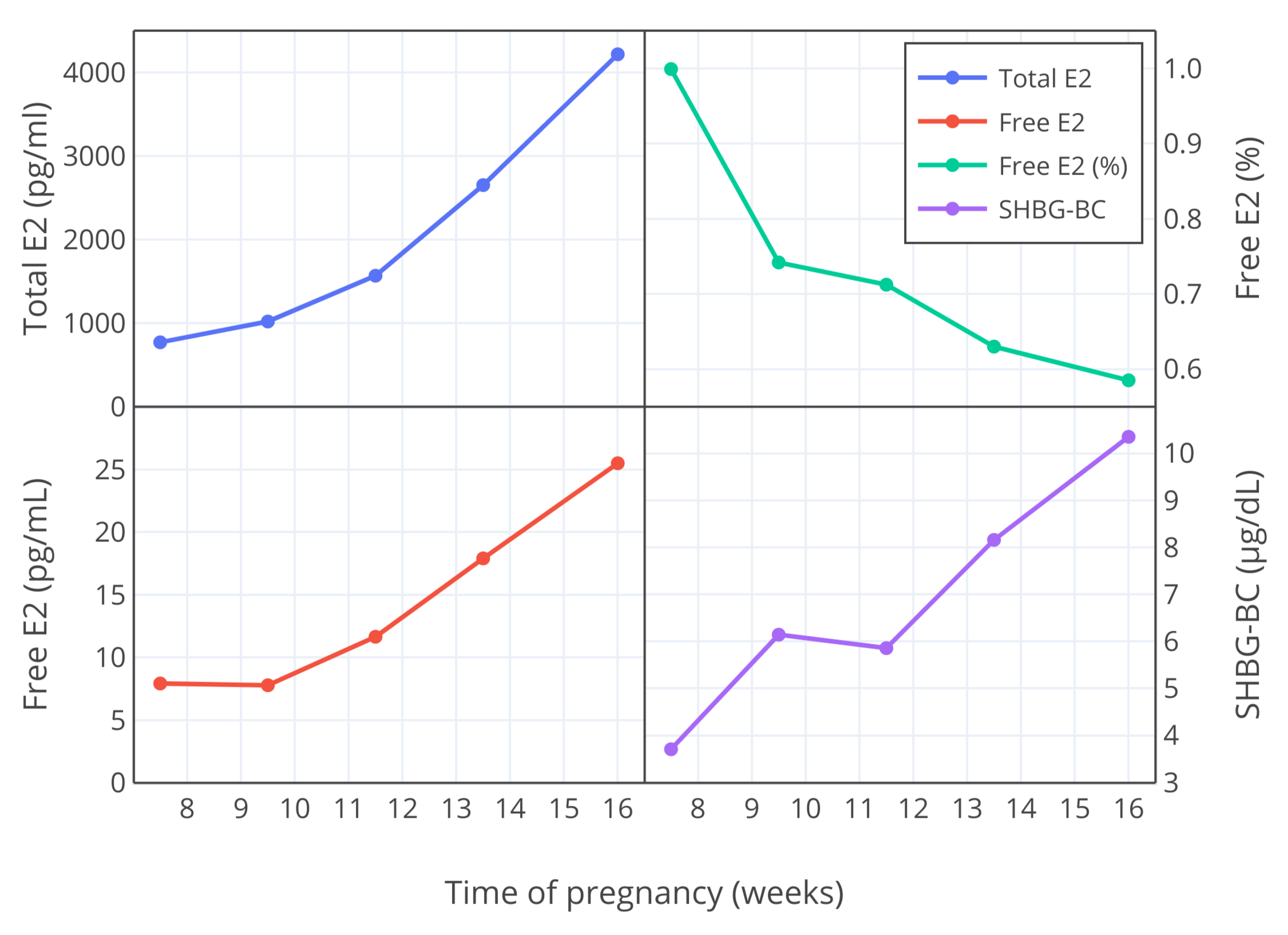
图 3:女性妊娠 7 到 16 周时,总雌二醇水平和游离雌二醇水平变化 (pg/mL),游离雌二醇百分比变化 (%) 和 SHBG 总量的变化 (μg/dL)(Bernstein et al., 1986)
妊娠期间,游离雌二醇可以用总雌二醇水平和 SHBG 水平计算。我粗略地算出了妊娠时游离雌二醇的百分比(使用了 O’Leary et al. (1991) 的数据和已出版的 Mazer (2009) 的电子表格计算器(Aly, 2020)。结果见下。
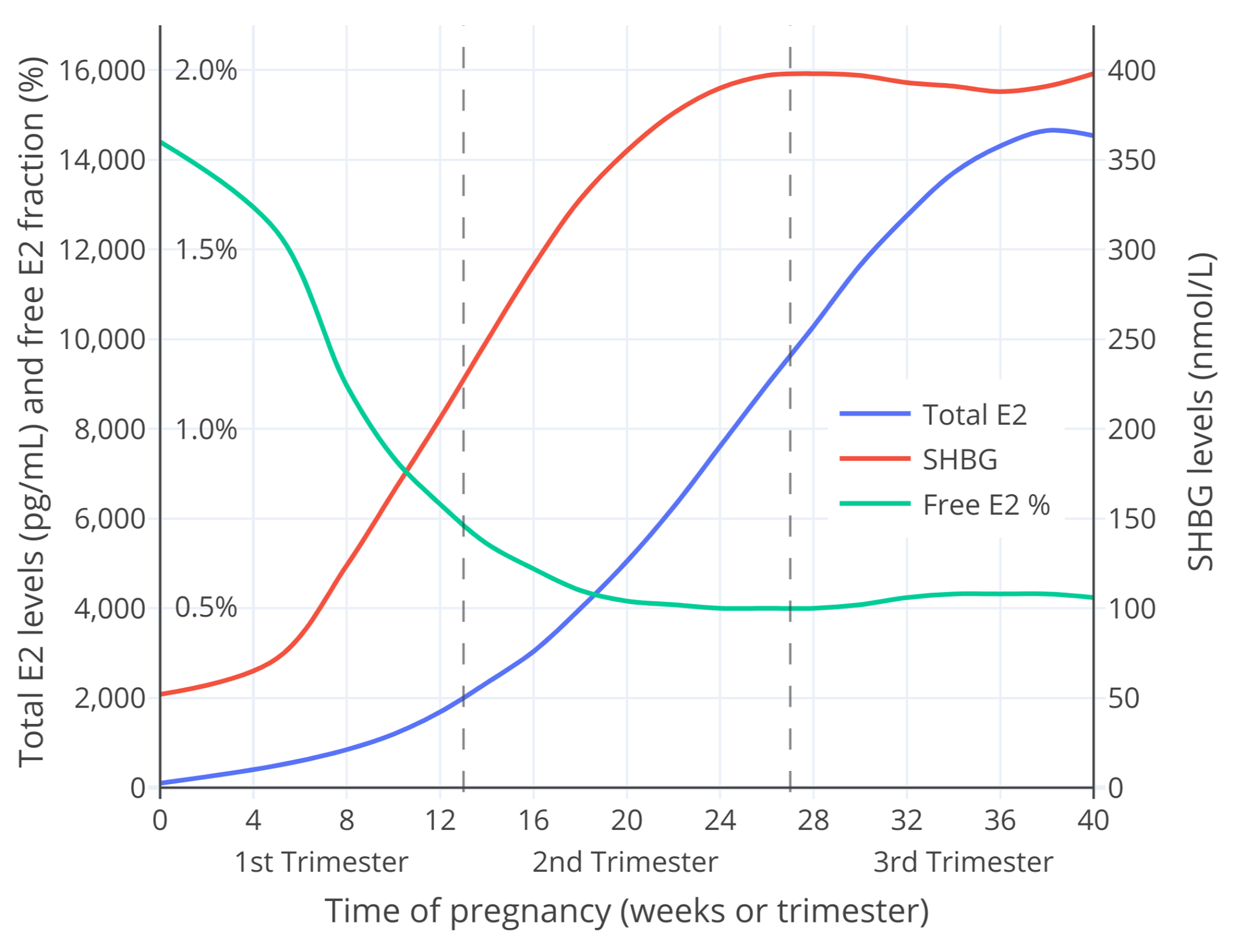
图 4:女性整个妊娠期测出的平均总雌二醇和总 SHBG 水平( O’Leary et al., 1991 )和计算出的游离雌二醇百分比( Mazer, 2009 )。这幅图还有另一个缩放到第一孕期的版本(雌二醇水平通常 ≤2,000 pg/mL )(图)
图中的游离雌二醇百分比仅仅是粗略的估计值,因此,应当保守考虑。不管怎么说,它们近似于现有的关于妊娠早期测量的游离雌二醇,如在数量级(相较于 Bernstein et al.)和整个孕期的变化方式(相较与 Bernstein et al. 和 Freymann et al. 两者)。由此,这些算出的值提供了一个可信的,重要的模型。
总的来讲,妊娠期间,总雌二醇水平极大地增加,与之相称地,SHBG 的增长虽相对较低但仍巨大。由于大量增长的 SHBG 水平,游离雌二醇的百分比在整个孕期逐步降低。现有的研究就游离雌二醇的百分比降至何种程度有所矛盾。不管怎样,妊娠后期游离雌二醇的可能百分比的范围约是 0.5 到 1.5% 。这些数值可与非孕期的游离雌二醇百分比 1.5 至 2.1% 进行比较。这相当于妊娠后期的游离雌二醇百分比最多降低到非孕期的 60% 左右。极端情况下,可能只降到非孕期时的 25% 左右。相反地,妊娠早期时,游离雌二醇相对较低,游离雌二醇的百分比更高。
尽管游离雌二醇百分比在孕期降低了,游离雌二醇水平和总雌二醇一样大量地增加了。这是因妊娠时增加的雌二醇水平明显地超出了一同升高的 SHBG 水平的限制作用。因这一原因,妊娠可以说是一种完全地超雌激素状态。
在妊娠期间,SHBG 并不像影响睾酮那样影响雌二醇,因为与之相称的雌二醇水平增长远大于 SHBG 水平的增长,雌二醇对 SHBG 的亲和力又相对较弱。一般而言,由于缺少大量的 SHBG 来面对更高的雌二醇水平这一内在要求,SHBG 不可能像限制睾酮那样限制雌二醇的活性。
口服雌二醇
当涉及到游离雌二醇时,口服雌二醇可能与非口服雌二醇不同。这是因为口服雌二醇要经历首过——这会使在肝脏中的雌二醇水平高于血液中的雌二醇水平。结果,口服雌二醇导致不相称的肝影响,使 SHBG 水平升至与其相称的比非口服雌二醇高的程度。因此,口服雌二醇带来的更高的 SHBG 水平可能会使游离雌二醇百分比比非口服的低。
虽然很可能是这样的,但就游离雌二醇而言,更难确定口服与非口服雌二醇之间差别的精确值。不过有一些数据。更年期的顺性别女性低剂量口服雌二醇的临床研究称,SHBG 增加的限制作用对所算出的游离雌二醇影响不大( Nilsson, Holst, & von Schoultz, 1984; Nachtigall et al., 2000 )。同样,与非口服雌二醇相比,口服雌二醇对更年期症状显示出相似的效果( Wiki; 第二段)。至于更高剂量的口服雌二醇,很少有提供 SHBG 水平或游离雌二醇水平的数据的研究。不管怎样,一项这样的研究发现,在跨性别女性中,6 mg/day 口服戊酸雌二醇(相当于约 4.5 mg/day 口服雌二醇)使 SHBG 水平增加了约 3.0 倍( Dittrich et al., 2005 )。使用这项研究中的总雌二醇和 SHBG 水平,可以粗略地算出( Mazer, 2009 )游离雌二醇的百分比可能从约 2.1% 降至 1.2% ( 43% 降低)。类似地,一项使用口服结合雌激素( CEEs; 倍美力)在使 SHBG 水平升高 2.3 倍的剂量下称,算出的游离雌二醇百分比相较于等剂量的透皮雌二醇(指总雌二醇水平)低 40% ( Shifren et al., 2007 )。这些发现表明,在女性倾向跨性别者的典型剂量的口服雌二醇下,游离雌二醇百分比会有个不容忽视的降低。所以,在同样的雌二醇水平下,口服雌二醇相较于非口服雌二醇可能在某种程度上没那么有效。
不过,我们必须明白,这一点并不确定。口服雌二醇的雌酮水平远比非口服雌二醇的高(约 5 倍)( Kuhl, 2005 ),而雌酮,虽不及雌二醇有效,也有类似于雌二醇的内在雌激素活性( Aly, 2019 )。我们不确定,雌酮会增加多少雌二醇的雌激素活性。不管怎样,雌酮很可能会显著地增加口服雌二醇的雌激素活性( Pande et al., 2019; Table )。这额外的雌激素暴露可能会潜在地起到弥补更高的 SHBG 水平带来的影响及口服雌二醇导致的降低的游离雌二醇百分比的作用。不过,需要进一步的研究来评估这一可能性。另一个考虑是,口服雌二醇带来的更高的 SHBG 水平除了降低游离雌二醇的百分比外,还能用来减少游离睾酮的百分比(甚至减少的比雌二醇还多)。这一点尤为重要,因为在女性倾向跨性别者中,抑制睾酮是雌二醇的一项关键的疗效,也是使用较高雌二醇水平的首要正当理由。由于类似于这些的可能性及性激素的游离水平仅表示其理论上的生物活性这一事实,我们不能想当然地认为口服雌二醇没有非口服雌二醇有效。只有进一步的临床研究,对比口服雌二醇和非口服雌二醇,才能阐明这一问题。
对女性化激素治疗的意义
一些女性倾向跨性别者担心 SHBG 可能会很大地限制雌二醇生效,从而妨碍女性化和/或乳房发育。一些人甚至声称,由于 SHBG 在较高的雌二醇水平时增加,高水平的雌二醇可能没有较低水平的有效。但是,这些观念很可能都是被误导的,都没有深入了解 SHBG 。这是因为就女性化和乳房发育而言,低雌二醇水平( <50 pg/mL )就足以完全起效—被顺性别女孩正常的和诱导的青春期( Aly, 2020 )及第二性征发育良好的患完全雄激素不敏症女性证实( CAIS )( Aly, 2020; Wiki )。现时,没有证据表明较高的雌二醇水平对女性化或乳房发育有益或不可或缺( Nolan & Cheung, 2020 )。事实上,现有的研究表明,女性倾向跨性别者在典型治疗水平的雌二醇下( 如 50–200 pg/mL ),雌二醇水平与乳房发育没有关联( de Blok et al., 2018; Meyer et al., 2020; de Blok et al., 2020 )。这与在较低雌二醇水平时就已确立雌二醇在女性化和乳房发育方面能起到的最大效果的概念相一致。因此,除了女性倾向跨性别者使用较高水平的雌二醇抑制睾酮外,对于缺乏雌激素暴露而致使不完全的女性化效果的担忧是站不住脚的。
不过,如果我们要探究 SHBG ,研究表明,SHBG 对游离雌二醇的限制作用—这很可能是雌二醇的生物活性—相当的大。在雌二醇的非孕期生理水平内(如 <200 pg/mL ),内源的或非口服的雌二醇对 SHBG 水平和游离雌二醇百分比的影响微小。不过,非常高的雌二醇水平对 SHBG 生产的影响比正常生理水平的雌二醇要大。妊娠期间,随着雌二醇大量增加,SHBG 水平最高也增加了 5 到 10 倍,游离雌二醇百分比可能会降至非孕期的 60% 。但妊娠时,实际的游离雌二醇水平却大量地增加了。不仅如此,SHBG 水平的增加和游离雌二醇百分比的降低在妊娠早期时低于妊娠后期。即使是非口服雌二醇通常会遇到的最高值,由 SHBG 引起的游离雌二醇百分比降低通常不大。这一减少的效果很容易就被稍微大的雌二醇剂量盖过。
前文只适用于非口服雌二醇,而口服雌二醇相较于非口服雌二醇而言,对 SHBG 生产的影响更大,因此口服雌二醇带来的较高的 SHBG 水平可能会造成比非口服雌二醇对游离雌二醇更明显的限制。认为这一游离雌二醇的减少相当与口服雌二醇的活性或效力的降低这种观念只是一种理论上的可能性而已。就疗效上讲,口服雌二醇已经证明其自身非常有效。低剂量的口服雌二醇下,游离雌二醇百分比降低得似乎不多。此外,虽然现时没有直接的比较,更高剂量的口服雌二醇似乎与非口服雌二醇一样,具有类似的抑制睾酮的效果。( Wiki; Graphs )。除了抑制睾酮外,现有的研究未曾发现口服与非口服雌二醇在效果(如乳房发育,女性化)上有任何差异( Sam, 2020 )。由此,口服与非口服雌二醇在 SHBG 水平和游离雌二醇百分比上的区别可能没有什么治疗意义。
除了降低游离雌二醇百分比,增加的 SHBG 水平也降低游离睾酮百分比,甚至降得更多。这对女性倾向跨性别者有利。
总之,女性倾向跨性别者不应该太担心因升高的 SHBG 水平而降低的游离雌二醇,不论非口服还是口服雌二醇。
附加素材
这篇文章的附加素材,见此处,包含一份电子表格和其他能估计游离激素的计算器(如 Mazer, 2009)。